Spitäler und Kliniken setzen bereits auf klinische Informationssysteme – es ist die Grundlage für das digitale Datenmanagement. Über den aktuellen Stand und die Trends schreibt unser Autor, der BFH-Medizininformatiker Jürgen Holm.
KIS 4.0 – Wohin geht die Entwicklung?
Die klinischen Informationssysteme (KIS) haben sich als die wichtigste Drehscheibe in den Spitälern etabliert. Sie stehen aber vor grossen Herausforderungen: ein Mehr an Prozesssicht, Einbindung wissensbasierender Systeme, integrierte Krankengeschichte, mobile Funktionsweise, Öffnung nach aussen und die Einbindung von Patienten in ihre Behandlung durch Datenerhebung.
Was bisher war
Der Umbruch der klinischen Informationssysteme ist in vollem Gang. In den vergangenen zwanzig Jahren stand vor allem die Frage der Integration vieler heterogener Abteilungssysteme zu einem konsistenten Gesamtsystem und der darauf basierenden Optimierung der Kommunikationsbeziehungen zwischen den verschiedenen Spitalbereichen im Vordergrund.
Intersektorale Anbindung nach aussen
Heute sehen sich MedizininformatikerInnen weltweit mit den Herausforderungen konfrontiert, die Informationssysteme (IS) eines Spitals nach aussen zu öffnen. Ziel ist es die IS in «eHealth-Landschaften» einzubetten. Dabei geht es z.B. in der Schweiz um die Anbindung der Spitäler an das elektronische Patientendossier [1] und dem Ausbau von B2B Beziehungen. In absehbarer Zukunft wird das Spital immer klarer als nur «ein» Akteur im Behandlungspfad der Patienten – von «Frau Brönnimann» [2] – sein. Managed Care und integrierte Versorgung werden immer grössere Versorgungsregionen oder eben eHealth-Gemeinschaften entstehen lassen, die mit B2B und B2C stark vernetzt sind. Die etablierten klinischen Systeme sind hier stark gefordert, den Anschluss nicht zu verlieren. Moderne Systeme drängen auf den Markt, die in diesem Punkt viel versprechen [3].
Prozessunterstützung
Weitere aktuelle Schwerpunkte sind die Funktionalitäten eines KISs über die reine Auftragskommunikation und medizinische Dokumentation hinweg, auf eine intelligente Prozessunterstützung (integrierte Krankengeschichte (KG)) mit wissensverarbeitenden Funktionen hin auszuweiten. Darüber hinaus ist bis heute auch die vertikale Integration von KIS in den einzelnen Spitälern nur mangelhaft umgesetzt [4]. Dies ist um so unverständlicher, als dass KIS eine grosse Anzahl an Informationen hat, die ein Managementinformationssystem für die wirtschaftliche und qualitative Steuerung eines Spitals dringend benötigen würden.
Helvetisierung
Medizinische Besonderheiten in der Dokumentation, Rollenverständnis zwischen Ärzteschaft und Pflegenden, Abrechnungen, Qualitätsanforderungen, neue Regularien und Gesetzesvorlagen und anderes mehr sind eine immer wiederkehrende (nationale) Herausforderung. Dies tritt besonders zutage, wenn neue Hersteller aus dem Ausland auf den Schweizer Markt drängen. Ohne geht es nicht – vor allem dann, wenn eine Prozesssicht umgesetzt werden soll, die auch im Zusammenspiel von ambulant und stationär funktionieren solle sowie in der Beziehung zu den gesetzlichen Qualitätsanforderungen und Krankenkassen.
Mobile KIS
Dass ein zunehmendes Bedürfnis der Gesundheitsfachpersonen besteht, die, die Arbeit auch – wo sinnvoll – mit mobilen Geräten wie Smartphones oder Tablet zu verrichten, steht ausser Frage. Nur das «Wie» ist schwer zu beantworten. Eine völlig neue Sichtweise auf die Datenrepräsentation ist hier zu nennen. Kontextbasierte Informationspräsentation aus dem KIS heraus erfordert nicht nur ein neues Denken zur Oberflächengestaltung, sondern auch den Einbezug von Sensoren, die Mitarbeiter, Patienten, Räume, Geräte usw. eindeutig identifizieren und dies den mobilen Applikationen mitteilt. Noch komplexer wird das Thema, wenn zusätzlich auch noch Daten erfasst werden sollen. Dies kann ebenfalls sensorbasiert teilautomatisiert umgesetzt werden, erfordert aber zusätzlich einfache Eingabemöglichkeiten durch das Personal. Die Erfassung und Visualisierung von pflegerischen sowie medizinischen Daten auf mobilen Geräten erfordert also eine entsprechend Systemarchitektur und ein neues Prozessdenken von den Herstellerfirmen und den AnwenderInnen!
Einbezug von «Frau Brönnimann»
Und Frau Brönnimann? Der Einbezug von PatientInnen in ihre Behandlung öffnet ganz neue Perspektiven – und Sicherheitsfragen. So gehen die Kliniken vermehrt dem Wunsch nach, die PatientInnen besser in ihre Behandlung einzubinden und sie damit auch besser an ihr Spital zu binden. Apps sind dabei die bevorzugte Herangehensweise. Insbesondere die Nachbetreuung spielt hier eine grosse Rolle. Z.B. ein postoperatives Monitoring, Nachsorge von onkologischen PatientInnen (beides Beispiele, die am Institute for Medical Informatics [5] an der BFH umgesetzt worden sind) oder die Einschätzung der Suizidalität von entsprechend diagnostizierten psychiatrischen Patienten.
Erkenntnisse
Besonders zwei aktuelle Medizininformatik-Entwicklungen im Gesundheitswesen – der Aufbau von eHealth-Communities [1] und der Einzug der digitalen Transformation (Health 4.0, Internet of Things) [6] – bieten viele Chancen für die prozessorientierte Weiterentwicklung der heutigen KIS.
Die Zusammenführung dieser Technologien dürfte einen grossen Synergieeffekt ausüben. Zu den Herausforderungen zählen u. a.:
- die Umsetzung regulatorischer Vorgaben im Kontext von eHealth Suisse
- die Erhöhung der Patientensicherheit durch eine verbesserte Sicht auf die Behandlungsabläufe
- der sachgerechte Einsatz internationaler Standards, insbesondere bei den Stamm- und Metadaten für einen interoperablen Informationsfluss
- die Konvergenz bestehender Technologien wie eHealth (Vernetzung), pHealth (personalisierte Gesundheitsdaten), mHealth (mobile Health), sowie aHealth (Automatisation) rund um eine digitalisierte Gesellschaft.
Um den Herausforderungen gerecht zu werden, braucht es neben grossen Anstrengungen seitens der Hersteller auch eine bessere strategische Wahrnehmung im Management. Es muss zwingend eine ICT-Strategie ausgearbeitet werden, die im Einklang mit der Unternehmensstrategie steht. Diese Strategie sollte die Ziele und Visionen für den Einsatz von ICT nicht nur im Hause, sondern auch bezüglich der Bedeutung als (wesentlicher) Teil innerhalb einer Versorgungregion beinhalten. So muss ICT als Garant für die Effizienz- und Effektivitätssteigerung in der Unternehmensstrategie verankert sein, die Prioritäten in Richtung Digitale Transformation gesetzt werden, die vor allem ja eine Transformation der Organisation ist. Zudem muss das Know-How aufgebaut werden, die Basisinfrastruktur und grundlegend das Datenmanagement angegangen werden als Basis für alle weiteren Prozessoptimierungen. Das KIS hat sich zu Recht als die wichtigste Drehscheibe in den Spitälern etabliert – nun muss diese Drehscheibe weitere Akteure einbinden und die Silos durch neues Prozessdenken aufbrechen. Nur dann verdient das neue KIS den Namen 4.0.
Referenzen
- https://www.e-health-suisse.ch/gemeinschaften-umsetzung/epd-gemeinschaften.html
- Holm J., Lehmann M. von Kaenel F., Brönnimanns in die Stube geschaut – Hochschuldidaktische Schriftenreihe 11, 2013
- https://www.epic.com/software
- Holm J., Lehmann M., Gasenzer R. Das Spitalinformationssystem als Erfolgsfaktor im Wettbewerb. Competence 5- 12-13, 2013
- https://www.ti.bfh.ch/de/forschung/institute_for_medical_informatics/institute_for_medical_informatics.html
- Widmer W., Schaffhuser K., Gesundheitswesen gestalten, careum Verlag, S. 110-134, 1. Auflage 2018
 Create PDF
Create PDF








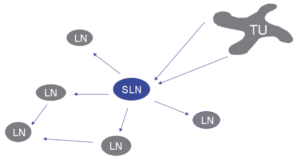 Abbildung 1: TU – Tumor, SLN – Wächterlymphknoten, LN – Lymphknoten
Abbildung 1: TU – Tumor, SLN – Wächterlymphknoten, LN – Lymphknoten

 Beiträge als RSS
Beiträge als RSS